Les médicaments prennent-ils notre santé à cœur ?
ÉVALUER LES RISQUES INHÉRENTS AUX MÉDICAMENTS APRÈS LEUR MISE EN MARCHÉ : UNE PRIORITÉD.E.S. Action Canada en collaboration avec Action pour la protection de la santé des femmes
Il est vrai que les médicaments contribuent largement à l'amélioration de la santé. Aujourd'hui, nous sommes en mesure de traiter des maladies autrefois incurables comme la méningite, la tuberculose et la syphilis. Nous disposons également d'analgésiques puissants dont le rôle est de soulager les derniers jours de patients atteints de cancer. Utilisés de façon appropriée, les médicaments peuvent faire la différence entre la vie et la mort, la souffrance causée par la douleur et le soulagement de celle-ci.
Il est également vrai que tous les médicaments présentent des effets secondaires. Des effets très différents de ceux qui sont causés par la maladie elle-même. Ces effets ont des conséquences qui vont d'un simple dérangement à des problèmes plus graves, voire irréparables, pouvant même entraîner la mort.
Certains médicaments présentent plus de risques que d'autres, mais il est toutefois impossible de fabriquer un médicament qui n'en présenterait aucun.
| Tous les médicaments présentent des effets secondaires. Prendre un médicament, c'est composer avec ses effets bénéfiques et ses effets indésirables. | |
|
Les décès imputés aux médicaments.
En 1998, des chercheurs de l'université de Toronto ont publié une étude portant sur la fréquence des réactions médicamenteuses graves chez les personnes hospitalisées et sur le nombre de décès s'y rattachant.
Ils se sont penchés sur des études américaines effectuées dans les hôpitaux au cours des 30 dernières années. Seuls les décès reliés à la consommation normale de médicaments ont été examinés : ni les surdoses ni les erreurs n'étaient considérées.
Les résultats de l'étude sont bouleversants. Les chercheurs ont estimé que les médicaments sont à l'origine de 75 000 à 100 000 décès par an aux États-Unis. En conséquences, les réactions indésirables aux médicaments se classeraient entre le quatrième et sixième rang des causes principales de décès. Si l'estimé le plus élevé se révélait exact, seuls les maladies du cœur, les cancers et les ACV (accidents cérébro-vasculaires) entraîneraient plus de décès. En se basant sur de telles données, on estime que la consommation de médicaments serait responsable chaque année de la mort d'environ 10000 canadiens.
La mise en marché d'un médicament au Canada : un processus trop secret
Pour faire approuver la vente d'un médicament sur le marché canadien, le fabricant doit au préalable effectuer des études sur les tissus et les cellules en laboratoire, puis sur les animaux et enfin auprès de volontaires afin d'en démontrer son efficacité et son innocuité.
La Direction générale des produits de santé et des aliments (DGPSA) de Santé Canada examine la demande de la compagnie et décide de la mise en vente du médicament le cas échéant. Si le médicament est approuvé, la DGPSA approuve également l'étiquetage spécifique devant l'accompagner.
Cette étiquette inclut : le mode d'emploi du médicament, les problèmes qu'il traite de manière efficace, des avertissements concernant ses effets indésirables possible, son interaction avec d'autres médicaments et de l'information quant aux personnes qui devraient ou non prendre le médicament - ce médicament convient-il aux enfants, aux personnes âgées, aux femmes enceintes ou aux personnes présentant certains problèmes de santé ?
Au Canada, ces décisions sont prises à huis clos. Ni la population ni même les médecins n'ont accès aux rapports des évaluateurs de la DGPSA pas plus qu'à ceux transmis par les compagnies pharmaceutiques concernant l'innocuité ou l'efficacité des médicaments. Lorsqu'un médicament reçoit une première approbation, il y a généralement peu d'études publiées sur l'efficacité et l'innocuité de ce médicament. Or, il est difficile, sinon impossible, de connaître les effets réels d'un médicament si on n'a pas accès aux études non publiées.
Pourquoi cette information est-elle tenue secrète au Canada ? Pour des raisons de confidentialité commerciale, invoque-t-on en haut lieu. Ce motif n'est pas justifié. Toutes les entreprises possèdent des brevets sur leurs produits qui les protègent de leurs compétiteurs. La sécurité publique ne devrait pas être un secret commercial.
Les États-Unis se sont doté d'une législation beaucoup plus stricte que le Canada sur la liberté d'information. Pourtant dans ce pays, le public peut consulter les registres contenant des informations non publiées sur la sécurité et l'innocuité des médicaments et des analyses fournies par les réviseurs de la " Food and Drug Administration " américaine (FDA), sans que cela affecte la confidentialité commerciale. Aux États-Unis, on tient des audiences publiques sur les médicaments soumis pour approbation.
Une fois lancés sur le marché, plusieurs effets indésirables des médicaments sont encore méconnus
Même si la population canadienne avait accès aux études non publiées de prélancement, la connaissance des effets indésirables des nouveaux médicaments serait somme toute limitée.
Habituellement, les essais cliniques sont effectués auprès de 2000 à 3000 personnes pendant de courtes périodes de temps. Après la mise en vente du médicament, il est possible que des milliers, voire des millions, de personnes le consomment. Quand seulement 2000 à 3000 personnes essaient un médicament, il est peu probable que des réactions indésirables graves soient découvertes et cela est d'autant plus vrai quand ces réactions touchent moins d'une personne sur 800, comme c'est souvent le cas.
En outre, différentes catégories de personnes peuvent le consommer, y compris des enfants ou des personnes âgées et il est possible qu'un médicament soit utilisé pendant des périodes prolongées. Par exemple, les études sur les antidépresseurs durent généralement de 6 à 8 semaines. Or ces mêmes médicaments sont prescrits des années durant! Il y a aussi un autre problème. Les mesures utilisées lors de ces études n'indiquent pas toujours les effets à long terme d'un médicament sur la santé d'une personne. Par exemple, une étude peut démontrer qu'un médicament diminue le taux de cholestérol ou la pression sanguine, sans démontrer les effets possibles sur les maladies cardiaques.
Les renseignements recueillis par les compagnies sur l'innocuité des médicaments dans les études de prélancement sont utiles, mais ils sont nettement insuffisants. Les compagnies désirent lancer leur produit rapidement sur le marché afin d'obtenir un rendement sur l'investissement consacré à sa mise au point. Cependant, il est important de savoir que les nouveaux médicaments lancés sur le marché, n'ont pas tous la valeur qu'on voudrait leur accorder. Selon le Conseil d'examen du prix des medicaments brevetés, sur 577 nouveaux produits analysés entre 1991 et 1997, seulement 8.7 % d'entre eux représentaient de réelles avancées thérapeutiques, 41.6 % offraient peu ou pas d'avantages par rapport aux produits déjà sur le marché et 49.7 % n'étaient que des produits dérivés de produits déjà existants (posologie différente ou autres changements mineurs).
| LA RÈGLE DES 5 ANS | |
Compte tenu du manque d'informations sur les risques entourant les nouveaux médicaments, le Public Citizen Health Research Group, un organisme américain à but non lucratif, faisait à ses membres la recommandation suivante :
|
Notre système de pharmacovigilance ressemble plutôt à de la pharmacosomnolence. Le nombre de réactions nocives sérieuses est plus que minimisé.
Lorsque les médicaments sont approuvés pour la vente, la surveillance « post-marketing » aussi appelée pharmacovigilance, est principalement exercée au moyen d'un système de rapports volontaires et spontanés sur les effets indésirables d'un médicament. Ces rapports sont généralement rédigés par les médecins. Il arrive que les pharmaciens, les infirmières ou d'autres professionnels de la santé soumettent des rapports et, plus rarement, les patients eux-mêmes.
Les médecins peuvent soumettre un rapport au Programme canadien de surveillance des effets indésirables des médicaments, à la Direction des produits de santé commercialisés de Santé Canada, ou au fabricant du médicament. Les compagnies sont obligées de signaler tous les effets indésirables graves à Santé Canada. C'est-à-dire : une réaction causant l'hospitalisation d'une personne ou la prolongation d'un séjour hospitalier, une réaction causant le cancer, des malformations congénitales, l'invalidité ou la mort. Cette définition met de côté un grand nombre de problèmes de santé qui peuvent résulter de la prise de médicament.
Une étude réalisée au Royaume uni et publiée en 1998 révélait que pour 100 réactions nocives aux médicaments observées chez les hommes, 160 étaient observées chez les femmes.
« En tant que médecin de famille, j'ai toujours été conscient de l'insuffisance de mes connaissances sur les effets indésirables des médicaments. Quand je prescris un médicament, par exemple, et que mon patient revient avec des rougeurs, je ne sais jamais s'il s'agit d'une réaction au médicament ou d'un effet de la maladie elle-même. J'ai essayé quelquefois de signaler ce que je croyais être une réaction au médicament, mais j'ai trouvé la procédure si lourde et si longue que j'ai abandonné la démarche. Je serais prêt à parier qu'il y a plusieurs généralistes dans mon cas et je suis porté à croire que les données concernant les effets indésirables des médicaments ne sont pas exactes et qu'elles ne reflètent pas la réalité au niveau clinique ».
- un médecin de famille, Colombie-Britannique
Suite à l'approbation d'un médicament : les rapports volontaires concernant ses réactions indésirables ne révèlent que la pointe de l'iceberg.
Au Canada, entre 1984 et 1994, environ 1400 décès causés par une réaction médicamenteuse indésirable ont été enregistrés. Ce chiffre correspond à environ 2 % de l'estimation réelle basée sur des estimations provenant d'études menées dans les hôpitaux. David Kessler, ancien commissaire de la Food and Drug Administration américaine, estime qu'aux États-Unis seulement 1 % des réactions indésirables liées aux médicaments sont rapportées.
Selon ces données, 98% des décès survenant à la suite de réactions indésirables aux médicaments ne seraient pas identifiés comme tels. Ce pourcentage augmente encore lorsqu'on examine les études effectuées dans les cabinets de médecins. Une étude française révèle que lorsque les médecins prêtent une attention particulière aux réactions indésirables aux médicaments, ils rapportent, pour une période donnée, 4500 réactions de plus qu'en temps ordinaire pour une période comparable. Les rapports sur les réactions indésirables aux médicaments ne révèlent que la pointe de l'iceberg. Il s'agit là d'un système d'avertissement important, mais insuffisant.
« Comment évaluer l'innocuité réelle des médicaments sans connaître l'étendue des réactions indésirables graves qu'ils peuvent causer ? Cela est aussi peu sensé que d'avoir une administration routière nationale sur la sécurité des transports qui ne disposerait d'aucun renseignement sur les accidents de voiture, ou une administration nationale d'aviation qui ne saurait pas le nombre d'avions à s'être écrasés. »
T. Moore, B. Patsy et C. Furberg, « Time to Act on Drug Safety », JAMA, 1998; 279 (19) : 1571-3.
Que fait Santé Canada pour améliorer le système de pharmacovigilance ?
Les responsables de Santé Canada savent que le système n'est pas efficace. Ils ont fait quelques changements dernièrement et en recommandent davantage.
La Direction des produits de santé commercialisés de Santé Canada, responsable de surveiller les réactions médicamenteuses nocives, publie dorénavant un bulletin et des rapports réguliers dans le journal de l'Association médicale canadienne. Celui-ci a pour objectif d'informer adéquatement les médecins des effets nocifs qui ont été rapportés au Programme canadien de surveillance des effets indésirables des médicaments, ou ceux qui ont été observés dans d'autres pays. Malheureusement, il ne suffit pas à informer la population.
En 1997, Santé Canada a adopté un nouveau type d'approbation des médicaments : l'Avis de conformité conditionnel. Celui-ci oblige les compagnies pharmaceutiques à effectuer systématiquement des études suite à l'approbation d'un médicament pour la vente. Toutefois, ce type d'approbation est rarement utilisé. Cette mesure a été adoptée à titre de compromis, afin de lancer certains médicaments plus rapidement sur le marché comme des médicaments contre le SIDA par exemple, alors qu'on en connaît encore bien peu sur leur efficacité ou leur innocuité.
Santé Canada envisage actuellement d'apporter des modifications au système d'approbation en vertu desquelles les compagnies seraient obligées de soumettre des rapports d'innocuité tous les six mois pour les nouveaux médicaments et ce, pendant les trois premières années suivant l'obtention de leur licence. Ces rapports devront être plus complets qu'ils ne le sont actuellement. Ils seront néanmoins toujours fondés sur les rapports volontaires des réactions indésirables soumis à la compagnie et ne révéleront une fois de plus que la pointe de l'iceberg.
Les changements proposés par Santé Canada ne sont pas suffisants. Une surveillance systématique doit être exercée sur tous les nouveaux médicaments, non pas à titre de compromis pour tenter de compenser une réglementation trop faible mais bien pour améliorer les normes actuelles.
Comment améliorer le système de pharmacovigilance une fois les médicaments lancés sur le marché ?
RECOMMANDATIONS :
- RÉORGANISER le système d'approbation des médicaments afin que les nouveaux produits ne puissent être mis en vente au Canada que lorsqu'ils font preuve d'avantages thérapeutiques supérieurs au plan de l'innocuité, de l'efficacité, de la commodité par rapport aux médicaments déjà présents sur le marché. Ce processus doit être participatif et la population doit pouvoir avoir accès à l'information sur l'innocuité et l'efficacité des médicaments utilisée par Santé Canada et connaître de cette façon les raisons pour lesquelles Santé Canada a accepté ou refusé un nouveau médicament.
- ÉNONCER des règles de conduite détaillées et précises sur les conflits d'intérêt possibles, à l'intention des membres des comités scientifiques consultatifs et décisionnels impliqués dans la réglementation des médicaments. Tout individu ayant des liens financiers avec une entreprise manufacturière ne devrait pas être impliqué dans les décisions concernant l'approbation d'un médicament fabriqué par cette entreprise.
- UNE FOIS que le médicament est approuvé, veiller à ce que des études de suivi systématiques conçues selon des principes scientifiques soient entreprises au cours des premières années de son utilisation. Ces études doivent avoir comme objectif principal l'obtention de l'information nécessaire sur l'innocuité du médicament lorsqu'il est utilisé par une population nombreuse et dans des conditions relativement incontrôlées. Cette mesure ne devrait pas constituer un compromis pour affaiblir les critères d'approbation déjà en vigueur.
- RENDRE obligatoire pour les médecins, les pharmaciens et les autres professionnels de la santé le signalement des réactions indésirables aux médicaments. Encourager la participation au programme de pharmacovigilance dans le cadre des programmes d'enseignement.
- UTILISER les bases de données informatiques existantes seulement pour la surveillance routinière moins intensive des effets des nouveaux traitements médicamenteux sur la santé. Il est important de maintenir la confidentialité et de protéger la vie privée.
- METTRE au point un système d'avertissement efficace afin de faire connaître aux professionnels et à la population toute possibilité de réaction indésirable, ainsi que l'interdiction ou la restriction d'un médicament dans un autre pays en raison de ses risques pour la santé.
- ENTREPRENDRE des études spécifiques sur l'innocuité des médicaments consommés pendant la grossesse et l'allaitement et les médicaments utilisés par les femmes en bonne santé pendant des périodes prolongées. Ces études devraient porter sur le long terme aussi bien que sur le court terme.
- METTRE sur pied un processus d'approbation pour permettre à un nombre représentatif de femmes militant dans des organismes en matière de santé, de participer à l'évaluation et à l'approbation de nouveaux produits destinés d'abord aux femmes. Ceci devrait inclure tout nouveau produit hormonal pour femmes, mais sans se limiter à cette catégorie.
- ÉTANT DONNÉ le problème de la médicalisation inutile des différents cycles de vie des femmes (les menstruations, la ménopause, la grossesse et l'allaitement), entreprendre une révision publique exhaustive de tous les médicaments destinés à ces fins et disponibles actuellement sur le marché canadien. Il faudrait aussi une révision de tous les médicaments préventifs destinés aux femmes en santé (prévention de l'ostéoporose par exemple), et de tous les médicaments conçus pour le traitement de problèmes de santé mentale (médicaments pour combattre l'anxiété, somnifères et antidépresseurs).
- CETTE RÉVISION devrait se faire avec l'entière participation des organismes de femmes, comme nous l'avons décrit plus haut. Le but de cette révision serait de réexaminer les autorisations accordées et l'étiquetage des produits, et de développer de nouvelles politiques pour traiter les problèmes courants et futurs causés par la prescription inutile de médicaments destinés aux femmes.
Cette brochure publiée par D.E.S. Action Canada, en collaboration avec Action pour la protection de la santé des femmes, vise à sensibiliser la population à l'importance d'une surveillance rigoureuse des médicaments après leur mise en marché.
Cette brochure est le premier d'une série de publications examinant les nouveaux enjeux en matière de protection de la santé. Santé Canada procède actuellement à la refonte de la législation fédérale en matière de protection de la santé, incluant notamment la Loi sur les aliments et drogues et les lois sur les contaminants environnementaux. Alors que les intérêts des secteurs pharmaceutique, biotechnologique, alimentaire, chimique et nucléaire sont bien représentés à Ottawa, il est maintenant fondamental que les voix des citoyens et des citoyennes soient entendues. La grande priorité de la législation canadienne doit être celle de la « protection de la santé ».
------------------------------------------------------------------
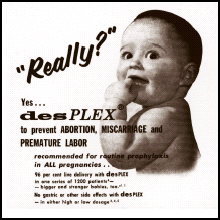 Le D.E.S. (diéthylstilboestrol) est l'un des pires désastres en matière de sécurité des médicaments. Au Canada, entre 200 000 et 400 000 femmes enceintes et leurs enfants ont été inutilement exposés à un médicament qui a eu des conséquences tragiques.
Le D.E.S. (diéthylstilboestrol) est l'un des pires désastres en matière de sécurité des médicaments. Au Canada, entre 200 000 et 400 000 femmes enceintes et leurs enfants ont été inutilement exposés à un médicament qui a eu des conséquences tragiques.
Le D.E.S est le premier oestrogène synthétique. Entre 1941 et 1971, il a été prescrit aux femmes enceintes en Amérique du Nord (plus longtemps en Europe) pour prévenir les fausses couches. Bien que des études effectuées sur les animaux avaient fait la preuve que le D.E.S. était lié au cancer :
- Il a été prescrit à des millions de femmes dans le monde entier.
- Il a continué à être prescrit durant la grossesse alors que son inefficacité avait été constatée près de 20 ans auparavant.
- Il a été reconnu comme étant la cause d'un cancer gynécologique 30 ans après qu'il ait été prescrit pour la première fois.
------------------------------------------------------------------
Recherche et rédaction :
Barbara Mintzes.
Conception et révision :
Rosanna Baraldi.
Information disponible sur les thèmes suivants : la publicité directe aux consommateurs des médicaments d'ordonnance, l'harmonisation internationale des réglementations sur les nouveaux médicaments, la prévention médicamenteuse de la maladie.
Pour mieux connaître Action pour la protection de la santé des femmes et pour obtenir la bibliographie complète, consulter le site web : http://www.whp-apsf.ca ou écrivez au APSF, Boîte postale 291, Station Q, Toronto (Ontario) M4T 2M1.
Pour plus d'information sur le D.E.S., consulter le site web de D.E.S. Action Canada : http://www.web.net/~desact
Ce projet a été rendu possible grâce au financement provenant du Centre d'excellence pour la santé des femmes de l'Université York et du Bureau de santé des femmes de Santé Canada. Les points de vue exprimés dans ce document ne représentent pas nécessairement la politique officielle de Santé Canada.
Copyright © D.E.S. Action Canada, 2000. Deuxième édition, 2003.
Droit d'auteur © 2006-2010 Action pour la protection de la santé des femmes

