Lettre de plainte à Santé-Canada: Pfizer publicité "étiquette pour l'orteil"
Le 14 mai 2004
L'honorable Pierre S. Pettigrew
Ministre de la Santé, ministre
des Affaires intergouvernementales
et ministre responsable des langues officielles
Chambre des communes
Édifice Confédération, bureau 507
Ottawa (Ontario)
K1A 0A6
Monsieur le ministre,
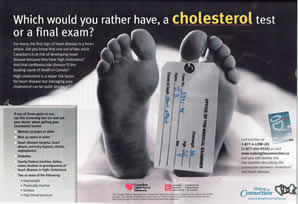
Devrait-on permettre à une société pharmaceutique de promouvoir son produit en donnant de l'information trompeuse sur les risques d'affections cardiovasculaires et en jouant sur la crainte de mourir d'une cardiopathie qu'éprouvent les Canadiennes et les Canadiens ?
Dans une lettre adressée à la rédaction du Lancet, en août 2003, le directeur et le personnel du service des médicaments essentiels et de la politique pharmaceutique de l'Organisation mondiale de la santé (OMS) ont exhorté les autorités sanitaires à « redoubler de vigilance en matière de publicité sur les médicaments ». Pour étayer leur demande pressante, ils citaient la campagne publicitaire menée récemment par Pfizer, en France, vantant les mérites du Lipitor, un médicament hypocholestérolémiant à base d'atorvastatin. Le docteur Jonathan Quick et ses collègues de l'OMS ont déclaré qu'il y avait, dans la campagne publicitaire, « des énoncés trompeurs et des omissions qui pouvaient soit inciter les gens à prendre ce médicament sans raisons médicales, soit entraîner des risques inacceptables 1 ».
Depuis au moins 18 mois, ces publicités circulent au Canada dans certains magazines et à la télévision. Des particuliers ont déposé des plaintes auprès de l'organisme Normes canadiennes de la publicité (NCP). La version canadienne est financée par Pfizer, mais les annonces imprimées indiquent seulement - en petits caractères - que « la campagne est commanditée par l'une des sociétés pharmaceutiques canadiennes axées sur la recherche ». Les logos du Canadian Lipid Nurses Network et de l'Association canadienne du diabète sont bien plus visibles. Et les annonces télévisées sont tout aussi vagues sur le rôle que joue Pfizer. Ainsi, non seulement la campagne présente-t-elle de l'information trompeuse sur les risques d'affections cardiovasculaires, comme le faisait la campagne en France, mais elle dissimule le fait que le financement provient d'une société pharmaceutique.
Vous trouverez ci-joint un exemplaire de l'annonce parue dans le numéro d'octobre-novembre 2003 du magazine Healthy Woman, ainsi qu'une copie de la plainte envoyée à NCP par M. Terence Young, ancien député à l'Assemblée législative de l'Ontario et père de Vanessa Young, cette jeune femme de 15 ans qui est décédée après avoir pris du cisapride (Propulsid). Lorsqu'il a déposé sa plainte, M. Young a appris que s'il communiquait avec les médias, NCP n'examinerait pas sa plainte. M. Young n'est pas le seul à avoir déposé une plainte auprès de NCP.
Deux facteurs nous inquiètent profondément, qu'il y ait eu examen ou non. D'abord, le fait que l'annonce circule toujours; ensuite qu'on n'ait pris, à ce jour, aucune mesure de réglementation afin que l'entreprise retire son annonce ou corrige les faux renseignements qui y figurent.
Cette campagne est dangereuse à plusieurs égards. D'abord, on y exagère les risques d'hypercholestérolémie chez les personnes n'ayant jamais eu de maladies cardiovasculaires. Ensuite, la campagne minimise d'autres problèmes de santé importants, dont le tabagisme, l'obésité et le diabète, et omet de mentionner des activités de promotion de la santé (alimentation saine, exercices et réduction du stress, par exemple). En exploitant ainsi les craintes de la population, ces annonces inciteront sûrement certaines personnes à en consommer même si elles n'en ont pas besoin et n'en retireront aucun bienfait. Le message sous-jacent de cette campagne est le suivant : les personnes qui n'ont jamais souffert de maladies cardiovasculaires auparavant peuvent éviter une crise cardiaque fatale si elles suivent un traitement contre l'hypercholestérolémie. Or, ce message contredit les preuves scientifiques qui existent sur l'utilité de tels traitements. En voici un exemple : selon une étude méthodique des essais cliniques de m édicaments hypocholestérolémiants comme première ligne de prévention, les bienfaits au niveau cardiovasculaire étaient minimes. En outre, les essais ne semblent avoir eu aucun effet bénéfique sur la santé au chapitre de la morbidité, de l'hospitalisation, de l'invalidité ou des décès 2. L'étude signale également que seul un groupe d'hommes d'âge moyen a vu une légère amélioration de la santé cardiovasculaire, soit 28 % des sujets 3. Les médicaments n'ont eu aucun effet bénéfique chez les hommes âgés ou les femmes.
Financer ce type de publicité, que cet argent provienne du secteur public ou du secteur privé, est injustifié. En outre, cela accroît la demande pour des services de santé. Or, cet argent pourrait être mieux investi tant dans le secteur des services de santé que dans celui des déterminants de la santé.
Notre demande est simple : que le ministère de la Santé annule dès maintenant cette campagne publicitaire par des mesures de réglementation et impose des sanctions afin de prévenir d'autres infractions de ce genre. Le Ministère devrait aussi obliger Pfizer à effectuer, à ses frais, une campagne publicitaire correctrice dans les mêmes médias et de la même intensité que celle de la campagne en cours.
De plus, nous vous saurions gré de bien vouloir fournir des précisions sur les points suivants :
- les modalités de l'enquête que mènera le Ministère sur la campagne publicitaire; - l'échéancier;
- les mesures que prendra le Ministère durant l'enquête afin de protéger la population contre les messages trompeurs véhiculés dans les annonces;
- les décisions que vous prendrez et communiquerez à la société pharmaceutique.
Nous vous remercions de votre collaboration. Il incombe aux organismes de réglementation de veiller à ce que la population soit à l'abri d'informations trompeuses en matière de santé et de traitements médicaux, surtout celles qui exploitent les craintes que suscitent la mort et l'invalidité. Cette fonction a des retombées cruciales sur la santé publique.
N'hésitez pas à communiquer avec nous si vous avez des questions ou désirez de plus amples renseignements.
Renvois :
- Quick, Jonathan D. et al. Lettre à la rédaction, The Lancet, vol.362, n° 9385, 30 août 2003.
- « Do statins have a role in primary prevention? », Therapeutics Letter, n° 48, avril-juin 2003. http//www.ti.ubc.ca/PDF/48.pdf
- « Statin's benefit in secondary prevention confirmed: What is the optimal dosing strategy? » Therapeutics Letter n° 49, juillet-septembre 2003. http://www.ti.ubc.ca/PDF/49.pdf
Je vous prie d'agréer, Monsieur le Ministre, mes sentiments les plus respectueux.
Anne Rochon Ford
au nom du Comité de direction d'Action pour la protection de la santé des femmes :
Dr Ken Bassett, université de la Colombie-Britannique
Mme Sharon Batt, université Dalhousie
Mme Madeline Boscoe, Réseau canadien pour la santé des femmes
Dr Joel Lexchin, Université York
Dr Abby Lippman, Réseau canadien pour la santé des femmes
Dr Fiona Miller, Université McMaster
Dr Barbara Mintzes, université de la Colombie-Britannique
Mme Laura Shea, Sensibilisation au cancer du sein Montréal
et des membres affiliés d'Action pour la protection de la santé des femmes :
Wendy Armstrong, Consumers Association of Alberta
Dr Rosanna Baraldi, DES Action Canada
Dr Warren Bell, PharmaWatch
Wanda Cree, Seniors Community Health Council, Alberta
Janet Currie, PharmaWatch
Colleen Fuller, PharmaWatch
Brewster Kneen, Ram's Horn
Carol Kushner, PharmaWatch
Dr Peter Mansfield, Healthy Skepticism, Australie
Michael McBane, Coalition canadienne pour la santé
Kelsey Nortland, université Simon Fraser
Kathleen O'Grady, Université Concordia
Sharon Smith
Dr Jim Wright, Therapeutics Initiative, UBC
Pièces jointes :
copie de l'annonce lettre parue dans The Lancet Lettre de Terence Young copie des Therapeutics Letter n os 48 et 49 c.c. : * Dr Jonathan D. Quick, MPH, directeur du service des médicaments essentiels et de la politique pharmaceutique (EDM) de l'Organisation mondiale de la santé * M. Terrence Young, Drug Safety Canada * Mme Linda Nagel, présidente-directrice générale, Normes canadiennes de la publicité * Dr Chris Turner, chef de la Direction des produits de santé commercialisés, Santé Canada * Mme Anne Szukte-Fournier, coordonnatrice de la publicité, Direction des produits de santé commercialisés, Santé Canada * M. Ray Chepesiuk, Conseil consultatif de publicité pharmaceutique * Mme Deanna St. Prix-Alexander, directrice générale, Bureau pour la santé des femmes * Bureau de circonscription du ministre Pettigrew------------------------------------------------------
Résponse du Ministre de la santé, le 16 juin 2004. (9k PDF)
Droit d'auteur © 2006-2010 Action pour la protection de la santé des femmes

